これまで腎保護作用が期待される薬剤が数多く登場しては消えていきましたが、腎機能を守る本質的なアプローチは、腎虚血や腎鬱血といった血流障害をいかに防ぐかにあります。
①MAP(平均血圧)はいかなる時でも65mmHgを下回らないようにする
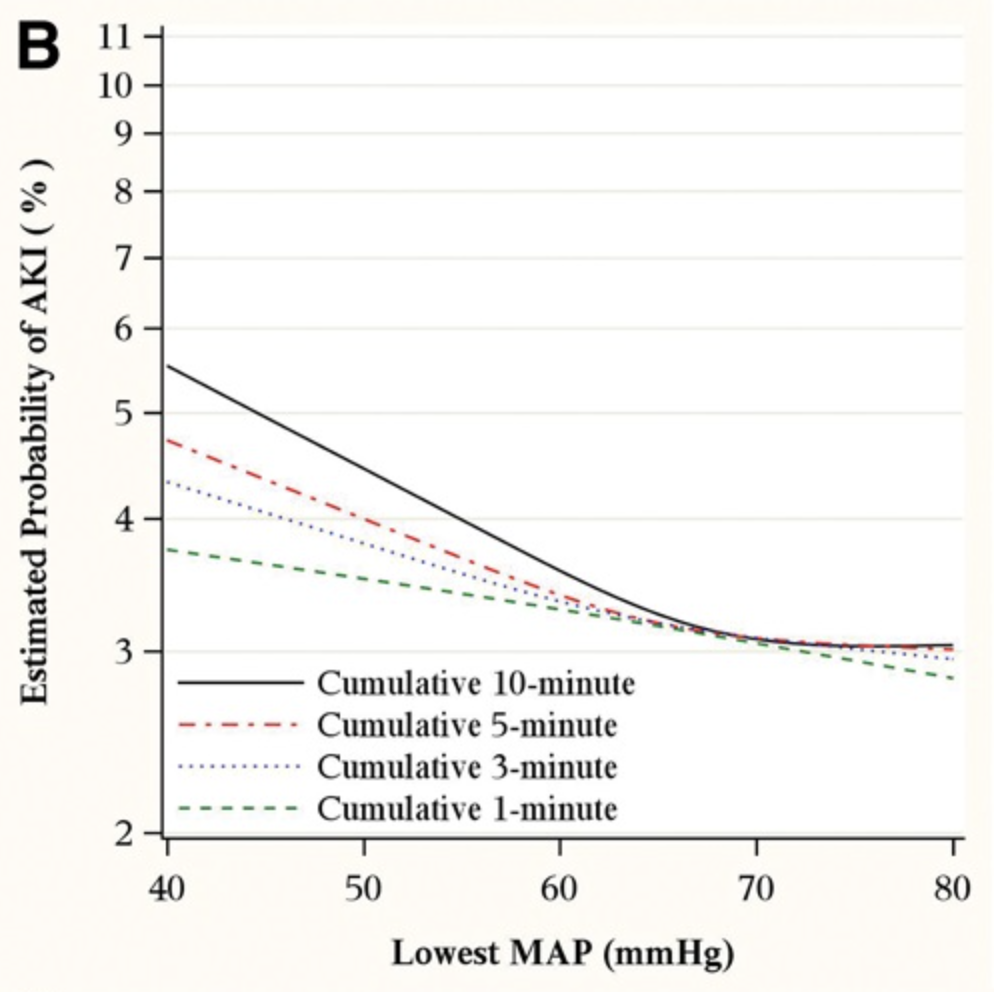
Anesthesiology 126(1):p 47-65, January 2017
このグラフは、低血圧とAKI発生率の関係を示したものです。平均動脈圧が65mmHgを下回ると、値が低くなるほど、そしてその状態が長く続くほど、AKIの発生率は顕著に上昇することがわかります。
できれば余裕を持って70mmHgは欲しいことも見て取れると思います。
臨床現場では、平均血圧が55〜60mmHg程度であれば、経過を観察する場面もあるかもしれません。しかし、ご覧のとおり、たとえ55mmHgの状態が10分間続いただけでも、AKIのリスクは確実に上昇します。特に、すでに腎機能が低下している患者では、このような低血圧により腎障害がさらに進行する可能性が高いと考えられます。
低血圧とBISの異常低値の発生の半分以上は麻酔開始から手術開始までの間に起こっている!
MAP65mmHg以下とBISの低値が重なると周術期死亡率が増加することはよく知られた事実ですが、
実は低血圧は執刀までに起こっている事が多いのです。多すぎる麻酔薬と他のことに気を取られている麻酔科医が昇圧を怠っている事が調査により判明しています。我々にとっては耳が痛い話ですが、真摯に受け止める必要があります。
麻酔導入前から昇圧剤の持続投与を始めて、手術開始直前に投与を一時終了しておく作戦
これだと、BISの値は下がってしまう事が多くても、低血圧だけは避けられます。
しかし、導入時に輸液を急速投与することは定番の対応策でしたが、現在では推奨されません。
②CO (心拍出量)の低下を避ける
患者さんの体の大きさを考慮したカーディアックインデックス(Cardiac Index)で2.2以下は心不全となり腎血流は確実に低下しますが、実はAKIのカットオフ値は未だ確立されていません。
心拍出量よりも平均血圧の方がAKIとの関連性が高い
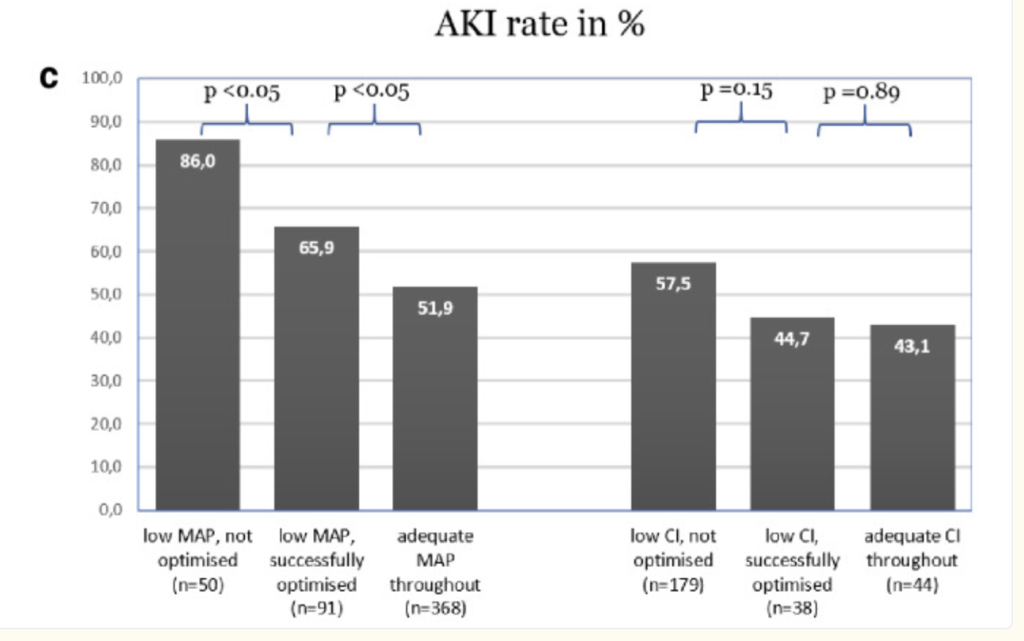
letter Intensive Care Med. 2021 Dec 18;48(2):242–245. doi: 10.1007/s00134-021-06601-0
向かって左の3本の棒グラフは平均血圧とAKIとの関係。右はCardiac IndexとAKIとの関係ですが
平均血圧の方がAKIと関連性が高い事がわかります。
ただし、Cardiac Index<3.0 はAKIのリスクは2倍になるようです。(麻酔科医にとってこの数字は結構、ハードルが高いですが、、、笑、一応知っておきましょう)
まとめますと、確かにMAPはCOよりもAKIと関連性は高いですが、COも大切です。
③中心静脈圧(CVP)は10mmHgを超えないように輸液をする
さて、腎保護というと脱水にしないというお答えが、すぐに返って来ると思いますが、
実は過剰な輸液投与もまた腎不全や他の臓器にも悪影響を与えてしまいます。
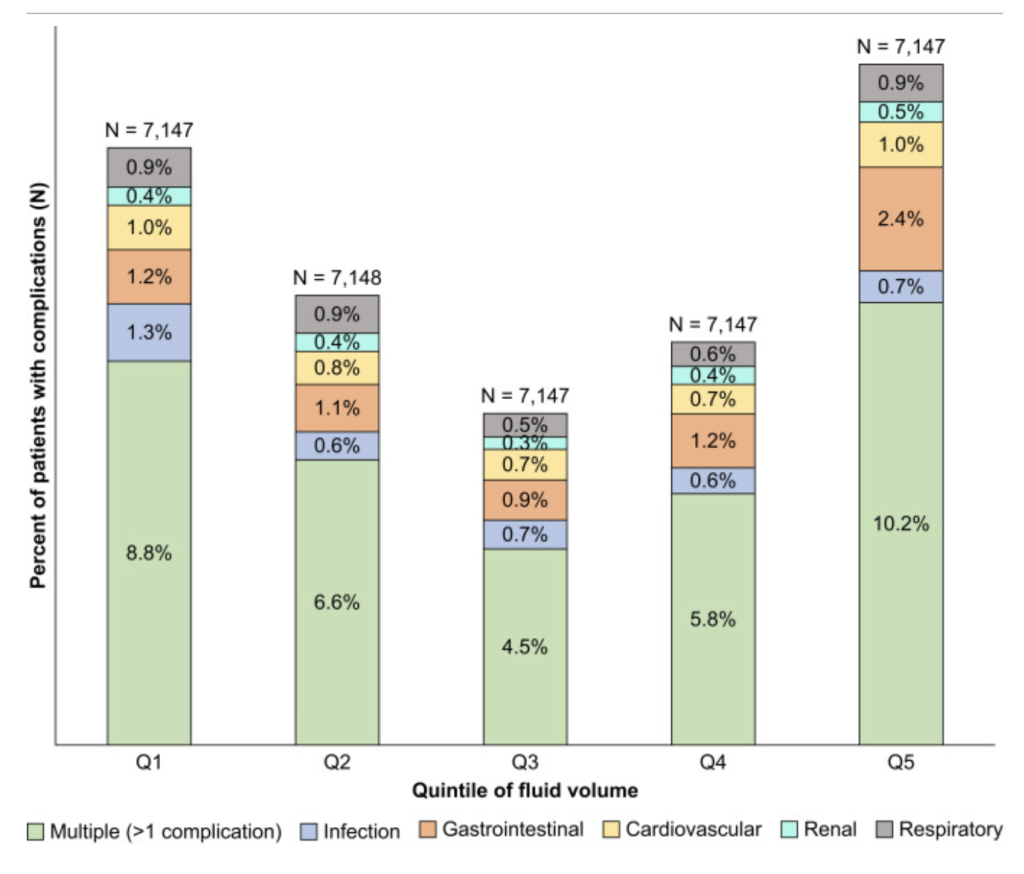
Association between perioperative fluid management and patient outcomes: a multicentre retrospective study 2021BJA
輸液量と合併症との関係性は全ての臓器でU字になっていることにご注目下さい。
少なくても多くても良くなく、適切な量の輸液管理を求められますが、
臨床医にとって、脱水の有無はある程度、身体所見や検査から把握しやすいものです。しかし、過剰な輸液や水分貯留といった「過剰状態」を正確に見極めるのは、むしろ困難であることが多いのではないでしょうか。
CVP↑→腎静脈圧↑ → 腎間質の圧迫 → 尿細管周囲の血流減少 → 腎血流のうっ滞と低酸素状態 → GFR低下
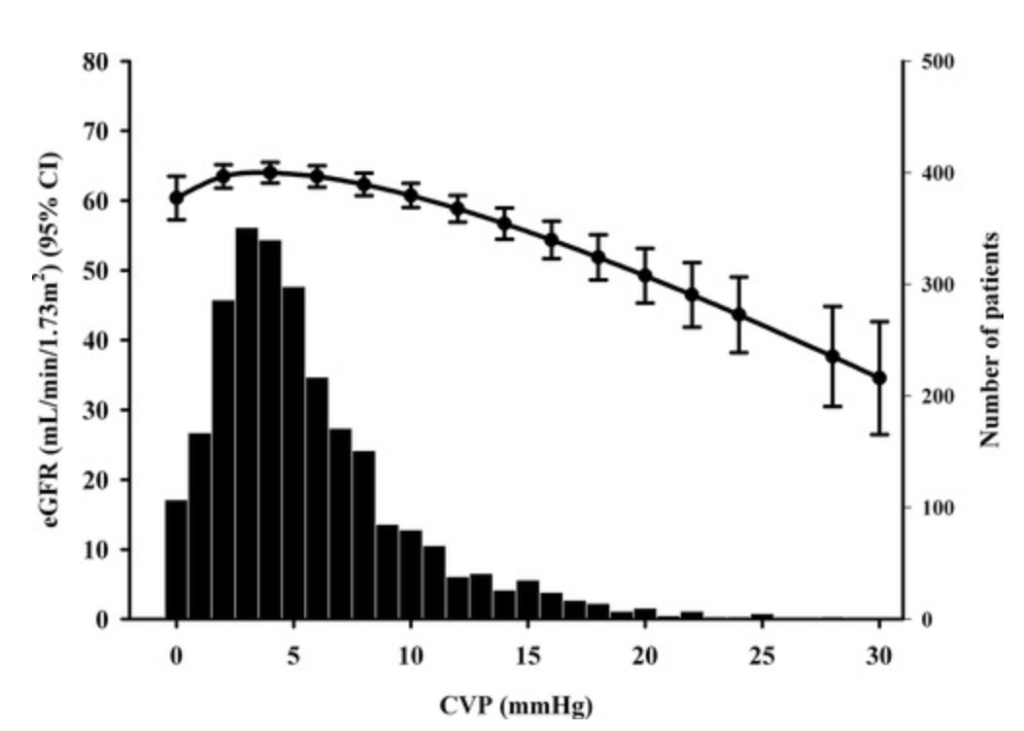
Increased Central Venous Pressure Is Associated With Impaired Renal Function and Mortality in a Broad Spectrum of Patients With Cardiovascular Disease JACC. 2009 Feb, 53 (7) 582–588
CVPが上昇するとGFRは低下して行くのがわかりますが、実際にAKIの発生率を疫学的に調査したスタディをご紹介します。
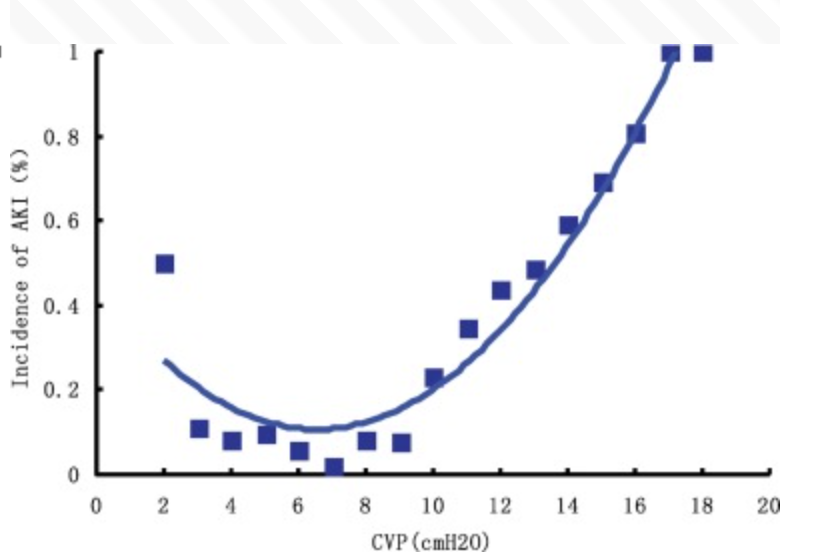
High central venous pressure is associated with acute kidney injury and mortality in patients underwent cardiopulmonary bypass surgery Journal of Critical Care, 2018-12-01, Volume 48, Pages 211-215,
CVPが10cmH2Oを超えたあたりから急激にAKIの発生率は上がっていくのがわかっていただけると思います。
レニン-アンギオテンシン-アルドステロン(RAAS)の関与
RAASはどう反応する?
通常、RAASは「腎灌流圧低下」に反応して活性化:
- 腎鬱血により有効腎血流量が減少 → 腎は「低灌流」と誤認
- その結果:
- レニン分泌↑
- → アンジオテンシンII↑
- → アルドステロン↑
CVP↑→アンジオテンシンII↑が引き起こす腎への悪影響(悪循環)
| 作用 | 結果 |
|---|---|
| 輸出細動脈収縮 | 一時的にGFR維持 → だが糸球体高圧持続で障害進行 |
| ナトリウム・水再吸収↑ | 体液過剰を助長 → さらにCVP↑ |
| TGF-βなどの線維化促進 | 腎間質線維化 → 慢性腎障害へ |
| アルドステロンによる心腎リモデリング | 心不全・腎不全を進行させる |
まとめ
AKI予防の戦略
- 平均血圧は一時的であっても65mmHgを下回らないこと(昇圧剤の持続が効果的)
- 輸液は充分にするが、CVPは10cmH2Oを超えないようにする
- CVPを計測出来ない時は、フロートラックのSVVが5を切らないように輸液する(次回、説明予定)